Conosci il grasso viscerale — quello attorno agli organi. Hai sentito del grasso epicardico — quello che avvolge il cuore. Ma esiste un terzo deposito adiposo, il meno conosciuto di tutti, che si nasconde dentro i tuoi muscoli. Si chiama IMAT (Intramyocellular Adipose Tissue, grasso intramuscolare). E nei pazienti con carcinoma mammario metastatico, ogni unità di aumento dell’IMAT si associa a una riduzione del 18% della sopravvivenza globale.
Non è un deposito visibile. Non lo vedi allo specchio, non lo sente la bilancia, non lo cercano gli esami di routine. Eppure la ricerca lo individua sempre più chiaramente come uno degli attori chiave nella prognosi oncologica.
Cos’è l’IMAT — e perché non è grasso “normale”
Il grasso intramuscolare è il tessuto adiposo che si infiltra tra le fibre muscolari scheletriche. Non va confuso con i trigliceridi intramiocelllulari (IMCL), che sono semplicemente depositi energetici fisiologici all’interno delle fibre muscolari — quelli che un atleta usa durante lo sforzo fisico.
L’IMAT è qualcosa di completamente diverso: è grasso patologico che occupa lo spazio tra le fibre muscolari, sostituisce progressivamente il tessuto muscolare sano e trasforma il muscolo in qualcosa che assomiglia — al microscopio e alla risonanza magnetica — alla carne marmorizzata.

IMAT (patologico)
Grasso infiltrato tra le fibre muscolari. Si accumula con invecchiamento, sedentarietà e obesità. Metabolicamente attivo, pro-infiammatorio, marker di rischio oncologico.
IMCL (fisiologico)
Trigliceridi energetici dentro le fibre muscolari. Aumentano con l’allenamento di endurance. Sono carburante per il muscolo, non un fattore di rischio.
L’IMAT si misura con risonanza magnetica (RM) o tomografia computerizzata (TC), analizzando l’area di attenuazione muscolare: le zone di bassa densità all’interno del muscolo scheletrico indicano l’infiltrazione adiposa. Non esiste un esame di laboratorio per rilevarlo.
Aumenta con l’invecchiamento, la sedentarietà e l’obesità — ma può essere presente anche in donne di peso normale. Uno studio del 2022 su 480 pazienti ha documentato valori di IMAT significativamente più alti nelle donne con carcinoma mammario rispetto ai controlli sani.
La sarco-obesità — la combinazione più pericolosa
La vera bomba oncologica non è l’IMAT da solo. È la combinazione di due fenomeni che spesso si presentano insieme: la sarcopenia (perdita di massa muscolare) e l’IMAT elevato. Questa combinazione si chiama sarco-obesità.
Il paradosso è inquietante: una paziente può avere un peso “normale” o persino un BMI nella norma, e allo stesso tempo avere poca massa muscolare funzionale e molto grasso infiltrato nei muscoli residui. La bilancia non lo vede. Lo vede la risonanza magnetica.
Una meta-analisi del 2024 ha dimostrato che la sarcopenia nelle pazienti con carcinoma mammario è associata a un 33% di aumento del rischio di mortalità e a un rischio triplicato di tossicità grave da chemioterapia. La prevalenza media di sarcopenia nelle pazienti con tumore al seno in stadio I–III è del 32,5%.
Studi di riferimento: Rier HN et al., Breast Cancer Res Treat 2017 (PMID: 28948392); Aro R et al., Breast Cancer 2024 (PMID: 38339347); Prado CM et al., Clin Nutr 2018 (PMC6221433).
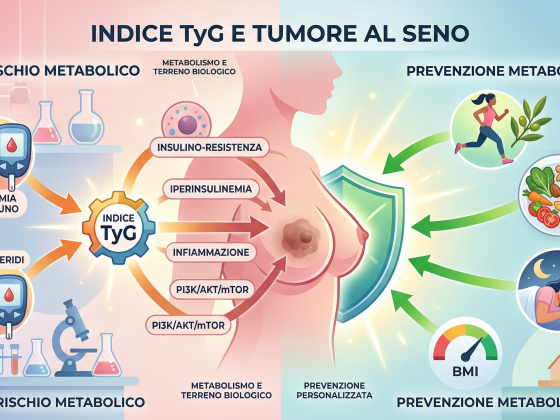
I 4 meccanismi con cui l’IMAT alimenta il tumore al seno
L’IMAT non è solo un marcatore passivo di cattiva salute muscolare. Attraverso quattro meccanismi distinti, contribuisce attivamente alla progressione del carcinoma mammario e peggiora la risposta alle cure.
1 Resistenza insulinica muscolare e asse IGF-1
Il grasso intramuscolare è un potente induttore di resistenza insulinica a livello del tessuto muscolare: secerne citochine infiammatorie e acidi grassi liberi che interferiscono direttamente con la segnalazione dell’insulina nelle fibre muscolari adiacenti.
Il risultato è un aumento compensatorio dei livelli circolanti di insulina e IGF-1. L’IGF-1 si lega ai recettori IGF-1R, sovra-espressi nelle cellule tumorali mammarie, attivando cascate di segnalazione che promuovono proliferazione cellulare e resistenza all’apoptosi — gli stessi meccanismi che rendono il tumore più aggressivo e più difficile da trattare.

Studi di riferimento: Tarnopolsky MA et al., Am J Physiol Endocrinol Metab 2019 (PMC6580171); Renehan AG et al., Lancet 2004 (PMID: 15221971); Farabaugh SM et al., Endocr Relat Cancer 2015 (PMC4335664).
2 Miochine alterate: meno irisina, più miostatina
Il muscolo sano non è solo un motore: è un organo endocrino che produce molecole protettive chiamate miochine. Quando il muscolo è infiltrato da grasso, questa funzione si deteriora in modo critico per due molecole chiave.
L’irisina — la miochina prodotta dall’esercizio fisico — ha effetti anti-tumorali documentati: riduce la proliferazione delle cellule MDA-MB-231 (triplo-negativo), ne inibisce la migrazione e potenzia l’effetto della doxorubicina. Un muscolo infiltrato da IMAT produce significativamente meno irisina.
La miostatina, al contrario, aumenta nel muscolo degenerato: favorisce l’atrofia muscolare, promuove l’infiammazione sistemica e crea un ambiente metabolico favorevole alla progressione tumorale.

Studi di riferimento: Provatopoulou X et al., J Biol Regul Homeost Agents 2014 (PMID: 25124080); Huh JY, Integr Med Res 2018 (PMID: 32393961); Patsalos O et al., Cancers 2021 (PMC8199282).
3 Tossicità da chemioterapia alterata
Questo meccanismo ha implicazioni pratiche immediate per le pazienti in trattamento.
La massa muscolare scheletrica è il principale compartimento di distribuzione per molti farmaci chemioterapici idrofili, tra cui gli agenti a base di platino e le antracicline. Una paziente con scarsa massa muscolare funzionale e alta infiltrazione di IMAT ha un volume di distribuzione ridotto: la stessa dose di farmaco produce concentrazioni ematiche più alte, esponendola a tossicità maggiore.
In parallelo, l’efficacia terapeutica si riduce: il farmaco non raggiunge le concentrazioni ottimali nel tessuto bersaglio. Il risultato è la combinazione peggiore possibile — più effetti collaterali e meno beneficio.
Implicazione pratica: valutare la composizione corporea (massa muscolare + IMAT) prima di calcolare le dosi chemioterapiche potrebbe ridurre significativamente la tossicità nelle pazienti sarcopeniche.
Studi di riferimento: Mallard J et al., Cancers 2022 (PMC9576176); Prado CM et al., Lancet Oncol 2009; Shachar SS et al., Breast Cancer Res Treat 2017 (PMC6221433).
4 Cachessia e ridotta risposta all’immunoterapia
L’IMAT è un marcatore precoce di cachessia neoplastica — la sindrome di deperimento che colpisce molte pazienti con carcinoma avanzato. Ma il suo ruolo va oltre il semplice marcatore: contribuisce attivamente al processo.
I muscoli infiltrati da grasso alterano il traffico dei linfociti T: le cellule immunitarie che dovrebbero combattere il tumore vengono dirottate o sequestrate nel microambiente muscolare infiammato, riducendo la risposta immunitaria anti-tumorale sistemica.
Questo ha conseguenze dirette per l’immunoterapia: le pazienti con sarcopenia e alto IMAT mostrano una risposta significativamente inferiore agli inibitori dei checkpoint immunitari (anti-PD-1, anti-PD-L1), proprio perché il sistema immunitario è già compromesso a monte dalla disfunzione muscolare.

Studi di riferimento: Barreto R et al., J Cachexia Sarcopenia Muscle 2022 (PMID: 36265324); Shafqat A et al., Front Oncol 2024 (PMC11083538); Brown JC et al., Cancer 2023 (PMC10000131).
Il dato clinico che nessuno ti ha ancora detto

Riduzione della sopravvivenza globale (OS)
per ogni unità di aumento dell’IMAT
nel carcinoma mammario metastatico
Un alto contenuto di IMAT è associato a una sopravvivenza globale peggiore con un hazard ratio di 2,21 (IC 95%: 1,70–2,86) nei tumori solidi — tra i più alti mai documentati per un parametro di composizione corporea.
Lo studio del 2022 su 480 pazienti ha documentato valori di IMAT significativamente maggiori nelle donne con carcinoma mammario rispetto ai controlli, indipendentemente dal BMI. Una meta-analisi 2024 conferma: la sarcopenia associata ad IMAT elevato è un predittore indipendente di prognosi negativa, sia in termini di sopravvivenza sia di tossicità terapeutica.
Cosa puoi fare — concretamente
La buona notizia: l’IMAT è reversibile. A differenza di molti fattori di rischio oncologico, risponde in modo significativo a interventi sullo stile di vita — in particolare all’esercizio fisico di forza e ad alta intensità.

-
Allenamento di forza (resistance training) — priorità assoluta
È la strategia più efficace per ridurre l’IMAT e costruire massa muscolare funzionale. Non bastano le passeggiate: servono esercizi con sovraccarico progressivo, almeno 2–3 volte a settimana. I benefici sono misurabili in 8–12 settimane.
-
HIIT per stimolare la produzione di irisina
L’allenamento ad alta intensità è il principale stimolo per la produzione di irisina — la miochina anti-tumorale. Anche 2–3 sessioni settimanali di 20 minuti producono un aumento misurabile di irisina circolante.
-
Proteine di qualità in quantità adeguata
Il muscolo per mantenersi e rigenerarsi ha bisogno di aminoacidi. L’apporto proteico raccomandato nelle pazienti oncologiche è di 1,2–1,5 g/kg di peso corporeo/die — significativamente più alto dello standard “normale” di 0,8 g/kg.
-
Chiedi una valutazione della composizione corporea
La DEXA avanzata o una TC già eseguita per staging possono essere rivalutate per misurare la massa muscolare e l’infiltrazione adiposa. Chiedi al tuo oncologo di includere la valutazione della composizione corporea nel tuo follow-up.
La medicina oncologica guarda il tumore. Guarda i marcatori tumorali, le dimensioni, i linfonodi, i recettori. Raramente guarda il muscolo — quello che rimane dopo mesi di chemioterapia, quello che fa da schermo immunitario, quello che distribuisce i farmaci.
L’IMAT è il deposito più sottovalutato di tutti. Non si vede, non si pesa, non si chiede. Eppure è lì — e la ricerca dimostra che la sua presenza parla chiaro su come andrà la malattia.
La cosa che mi colpisce di più, dopo 35 anni di medicina, è che la risposta a questo problema esiste e si chiama muscolo. Costruire muscolo di qualità è prevenzione, è cura, è sopravvivenza.
Il grasso nei muscoli non è un destino.
Il muscolo sano è una scelta — e la scienza è dalla tua parte.
Bibliografia
IMAT: Definizione, Origine e Misurazione
- Addison O, Marcus RL, Lastayo PC, Ryan AS. Intermuscular fat: a review of the consequences and causes. Int J Endocrinol. 2014;2014:309570. PMC: PMC3891754
- Srikanthan P, Gadgil M, Taksali S, et al. Intermuscular adipose tissue in metabolic disease. Nat Rev Endocrinol. 2023;19(2):82–95. PMID: 36564490
- Wan X, Xu M, Lin H, et al. Intermuscular adipose tissue in obesity and related disorders: cellular origins, biological characteristics and regulatory mechanisms. Front Endocrinol. 2023;14:1280853. PMC: PMC10619759
IMAT e Carcinoma Mammario
- Mallard J, Hucteau E, Hureau TJ, Pagano AF. Skeletal muscle deconditioning in breast cancer patients undergoing chemotherapy: current knowledge and insights from other cancers. Front Cell Dev Biol. 2021;9:719643. PMC: PMC9576176
- Rier HN, Jager A, Sleijfer S, Maier AB, Verhoef C, Meijer LJM. The prevalence and prognostic value of low muscle mass in cancer patients: a review of the literature. Oncologist. 2016;21(11):1396–409. PMC: PMC5785600
- Wu G, Xiao Y, Xu M, et al. High intramuscular adipose tissue content associated with prognosis and postoperative complications of cancers: a systematic review and meta-analysis. Front Oncol. 2024;13:1290485. PMC: PMC10751448
- Trinkner P, Widder J, Flury M, et al. A Nomogram Incorporating Intermuscular Adipose Tissue to Predict Chemotherapy Toxicity in Older Adults With Early-Stage Breast Cancer. J Clin Oncol. 2025. PMC: PMC12230286
Sarcopenia e Sarco-Obesità nel Carcinoma Mammario
- Aro R, Mäkinen N, Leinonen MK, et al. Sarcopenia in Breast Cancer Patients: A Systematic Review and Meta-Analysis. Breast Cancer Res Treat. 2024;203(2):201–14. PMID: 38339347
- Aleixo GFP, Shachar SS, Nyrop KA, et al. Myosteatosis and prognosis in cancer: systematic review and meta-analysis. Crit Rev Oncol Hematol. 2020;145:102839. PMID: 31841943
- Shachar SS, Williams GR, Muss HB, Nishijima TF. Prognostic value of sarcopenia in adults with solid tumours. Eur J Cancer. 2016;57:58–67. PMID: 26882087
Resistenza Insulinica Muscolare e Asse IGF-1
- Tarnopolsky MA, Rennie CD, Robertshaw HA, et al. Intermuscular adipose tissue directly modulates skeletal muscle insulin sensitivity in humans. Am J Physiol Endocrinol Metab. 2019;316(5):E866–79. PMC: PMC6580171
- Renehan AG, Zwahlen M, Minder C, O’Dwyer ST, Shalet SM, Egger M. Insulin-like growth factor (IGF)-I, IGF binding protein-3, and cancer risk: systematic review and meta-regression analysis. Lancet. 2004;363(9418):1346–53. PMID: 15121404
- Farabaugh SM, Boone DL, Lee AV. Role of IGF1R in breast cancer subtypes, stemness, and lineage differentiation. Front Endocrinol. 2015;6:59. PMC: PMC4335664
Miochine: Irisina e Miostatina
- Provatopoulou X, Georgiou GP, Kalogera E, et al. Effects of the exercise-inducible myokine irisin on malignant and non-malignant breast epithelial cell behavior in vitro. Cancer Lett. 2015;362(1):96–106. PMID: 25124080
- Patsalos O, Keeler J, Schmidt U, Loizou S, Loutradis D, Tchernof A. Exercise-Induced Irisin, the Fat Browning Myokine, as a Potential Anticancer Agent. J Clin Med. 2018;7(6):E129. PMC: PMC8199282
- Huh JY. The role of exercise-induced myokines in regulating metabolism. Arch Pharmacal Res. 2018;41(1):14–29. PMID: 32393961
IMAT, Tossicità da Chemioterapia e Farmacocinetica
- Prado CM, Baracos VE, McCargar LJ, et al. Sarcopenia as a determinant of chemotherapy toxicity and time to tumor progression in metastatic breast cancer patients receiving capecitabine treatment. Clin Cancer Res. 2009;15(8):2920–6. PMID: 19351764
- Shachar SS, Deal AM, Weinberg M, et al. Skeletal Muscle Measures as Predictors of Toxicity, Hospitalization, and Survival in Patients with Metastatic Breast Cancer Receiving Taxane-Based Chemotherapy. Clin Cancer Res. 2017;23(3):658–65. PMC: PMC6221433
Cachessia, Linfociti T e Immunoterapia
- Barreto R, Waning DL, Gao H, et al. Chemotherapy-related cachexia is associated with mitochondrial depletion and the loss of oxidative capacity in mouse skeletal muscle. J Cachexia Sarcopenia Muscle. 2022;13(3):1391–404. PMID: 36265324
- Shafqat A, Khan JA, Alkachem AY, et al. How Neutrophils Shape the Immune Response: Reassessing Their Multifaceted Role in Health and Disease. Int J Mol Sci. 2024;25(7):3856. PMC: PMC11083538
- Brown JC, Cespedes Feliciano EM, Caan BJ. The evolution of body composition in oncology. CA Cancer J Clin. 2023;73(1):44–65. PMC: PMC10000131
AVVERTENZE
Le informazioni contenute in questo sito sono solo a scopo didattico. Questo sito non fornisce e non può fornire consulenza medica. Non deve essere usato come sostituto delle cure mediche e dei consigli del tuo medico. Potrebbero esserci variazioni sul trattamento che il medico può raccomandare in base a fatti e circostanze individuali. La medicina è una scienza dinamica e dovrebbe essere considerata di conseguenza. Queste informazioni non devono essere utilizzate per diagnosticare o trattare alcuna
condizione. Non siamo responsabili per il modo in cui utilizzi e implementi le informazioni che ricevi. Questo sito è destinato all’uso solo da parte di adulti sani. Il Sito non è destinato all’uso da parte di minori, donne in gravidanza o individui con qualsiasi tipo di condizione di salute.
NON IGNORARE MAI I CONSIGLI MEDICI PROFESSIONALI A CAUSA DI QUALCOSA CHE HAI LETTO SU QUESTO SITO. NON AFFIDARTI MAI ALLE INFORMAZIONI CHE HAI RICEVUTO SU QUESTO SITO INVECE DI CERCARE UNA CONSULENZA MEDICA PROFESSIONALE. CONTATTA SEMPRE IL TUO MEDICO DI FIDUCIA E CHIEDI IL SUO PARERE SULLE INFORMAZIONI CHE LEGGI SU QUESTO SITO. NON APPLICARE CIO’ CHE LEGGI SU QUESTO SITO SENZA IL PARERE DEL TUO MEDICO DI FIDUCIA. NON UTILIZZARE QUESTO SITO PER LE EMERGENZE MEDICHE.